Ефективність
Ефективність
Препарат ПРЕВИМІС продемонстрував статистично значущу ефективність порівняно з плацебо1
Дані щодо ефективності ТГСК у реципієнтів, отримані до 24-го тижня1
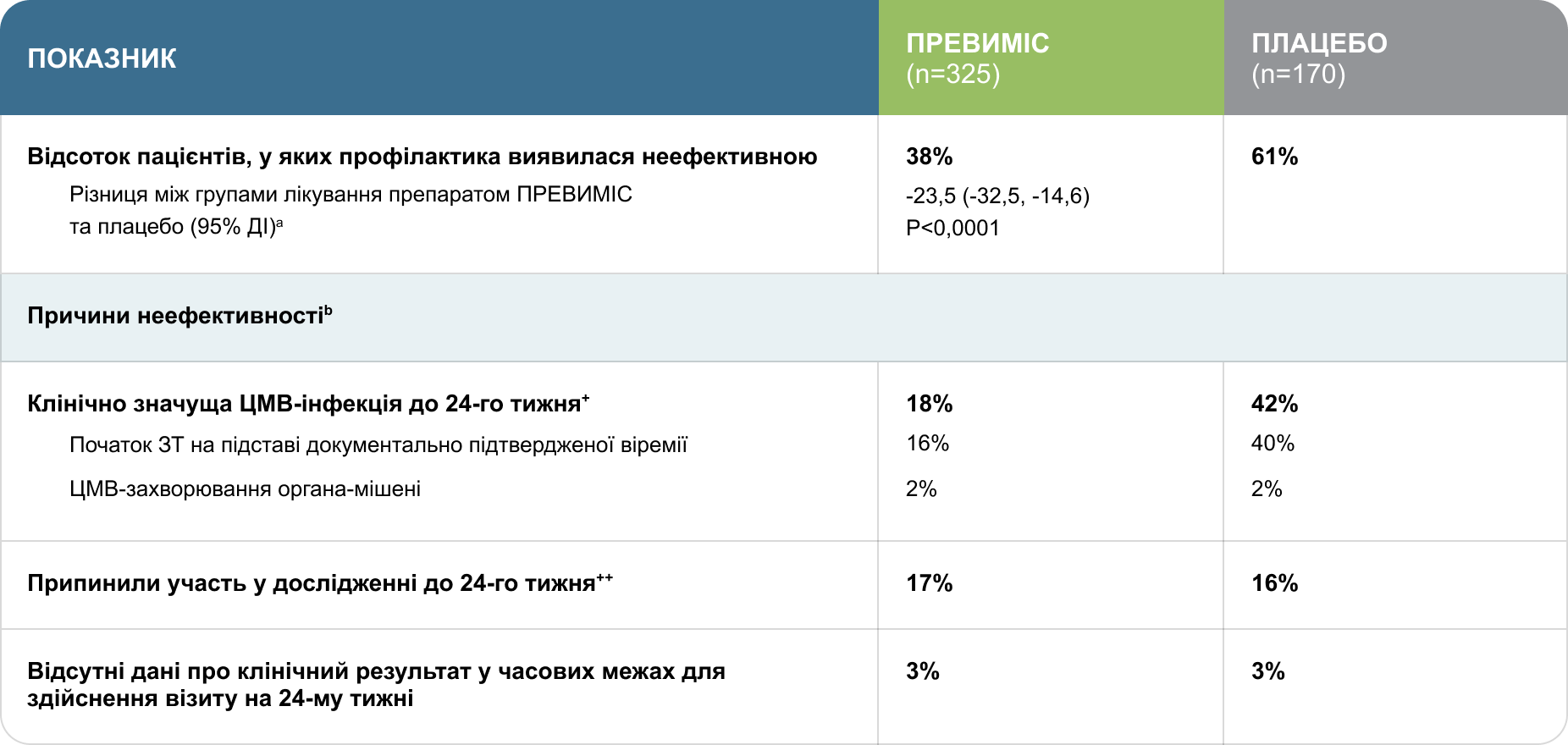
Первинна кінцева точка: клінічно значуща ЦМВ-інфекція*,c на 24-му тижні (підхід NC=F, популяція FASd)1
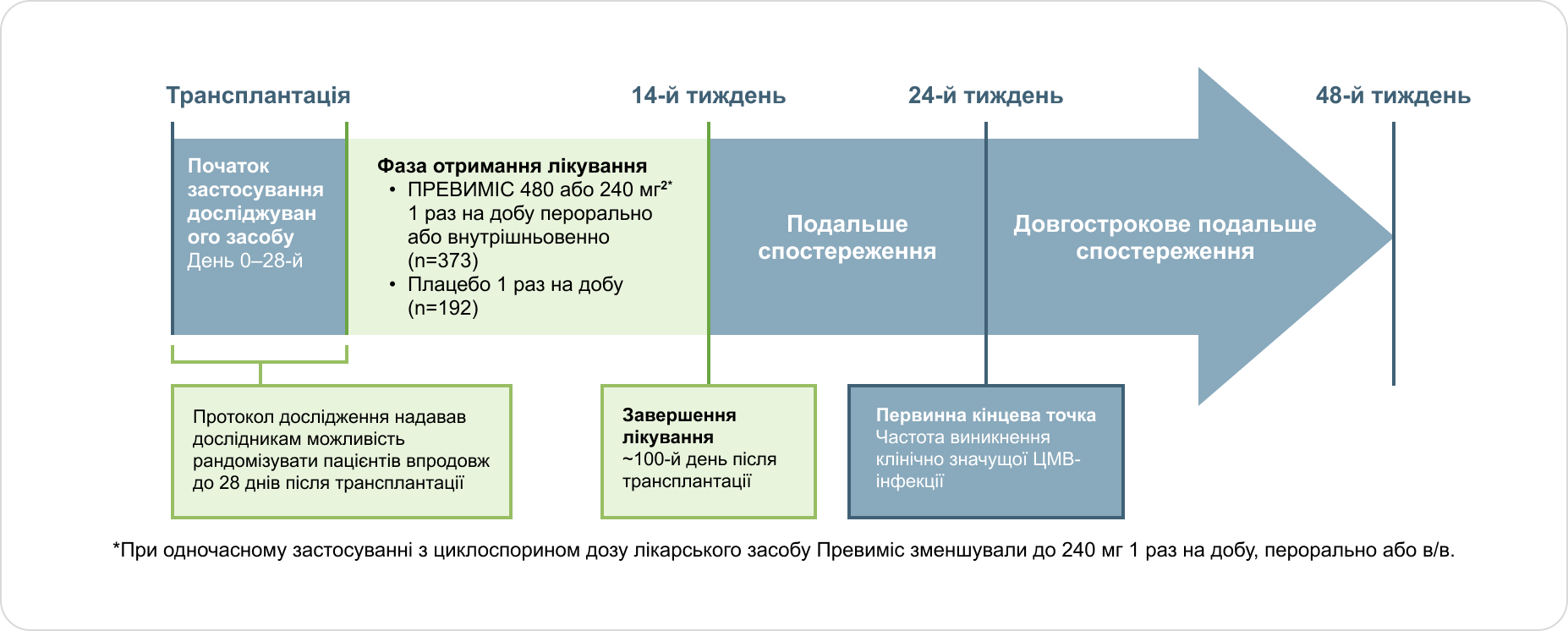
В учасників дослідження була розпочата профілактика після ТГСК (у будь-який час від 0 до 28-го дня після трансплантації, яка продовжувалася до 14-го тижня після трансплантації)1
Дизайн дослідження
Профілактика ЦМВ-інфекції оцінювалася у рандомізованому багатоцентровому подвійному сліпому плацебо-контрольованому опорному дослідженні ІІІ фази за участю дорослих ЦМВ-серопозитивних реципієнтів [R+] після алогенної ТГСК. Рандомізація проводилася зі стратифікацією за дослідницьким центром та рівнем ризику на момент включення у дослідження. Пацієнти були рандомізовані у співвідношенні 2:1 для отримання препарату ПРЕВИМІС або плацебо та стратифіковані за дослідницьким центром і рівнем ризику (високий чи низький) (N=565)1.
- Оцінювання смертності від усіх причин до 48-го тижня після трансплантації виконувалося як заздалегідь визначений пошуковий аналіз1
- Передбачені у протоколі рекомендації щодо порогових значень ДНК ЦМВ для початку ЗТ протягом періоду лікування становили ≥150 копій/мл або >300 копій/мл для пацієнтів, що належали до груп високого та низького ризику відповідно1
Огляд режимів хіміотерапії на вихідному рівні1

Додаткові характеристики популяції учасників дослідження1
- Середній вік становив 55 років (діапазон: від 18 до 76 років)
- 57% чоловіки; 43% жінки
- 84% європеоїди; 9% азійці; 2% темношкірі або афроамериканці та 7% іспаномовні етноси або латиноамериканці
- 48% пацієнтів отримували мієлоаблятивний режим
- 51% пацієнтів отримували циклоспорин та 43% пацієнтів — такролімус
*Під клінічно значущою ЦМВ-інфекцією розуміють або виникнення ЦМВ-захворювання органа-мішені, або початок анти-ЦМВ ЗТ залежно від ЦМВ-віремії та клінічного стану пацієнта.
+До 14-го тижня у 8% пацієнтів, які отримували препарат ПРЕВИМІС, та 39% пацієнтів, які отримували плацебо, виникла клінічно значуща ЦМВ-інфекція.
++Причини припинення участі у дослідженні включали побічні реакції, смерть, втрату для подальшого спостереження, рішення лікаря та вихід учасника з дослідження.
a95% ДІ та Р значення для різниці в лікуванні у відсотках відповіді були розраховані з використанням методу Мантеля — Хенселя з урахуванням стратифікації, з різницею, зваженою на середнє гармонійне розміру зразка для кожної групи (високий або низький ризик).
bКатегорії неефективності взаємовиключні та засновані на ієрархії категорій у зазначеному порядку.
cВіремія визначалася за допомогою тесту Roche COBAS® AmpliPrep/COBAS TaqMan®; нижня межа кількісного визначення становила 137 МО/мл, що дорівнює приблизно 150 копій/мл.
dFAS, популяція усіх пацієнтів для аналізу; FAS включає рандомізованих учасників дослідження, які отримали принаймні одну дозу досліджуваного засобу, і не включає учасників дослідження, у яких була виявлена ДНК ЦМВ на вихідному рівні. Підходи до поводження з відсутніми даними: підхід «не завершив курс, що прирівнюється до неефективності профілактики» (NC=F). При застосуванні підходу NC=F пацієнти з неефективною профілактикою визначалися як усі учасники, у яких розвинулася клінічно значуща ЦМВ-інфекція, або які достроково припинили участь у дослідженні, або щодо яких відсутні дані про клінічні наслідки у часових межах для здійснення візиту на 24-му тижні після трансплантації.
ДІ — довірчий інтервал; ДНК — дезоксирибонуклеїнова кислота; ЗТ — запобіжна терапія; ТГСК — трансплантація гемопоетичних стовбурових клітин; ЦМВ — цитомегаловірус
- Marty F.M., Ljungman P., Chemaly R.F. et al. Letermovir prophylaxis for cytomegalovirus in hematopoietic-cell transplantation. N Engl J Med. 2017; 377(25):2433-2444. DOI:10.1056/NEJMoa1706640
ПРЕВИМІС (летермовір), РП №UA/19168/01/01, №UA/19269/01/01